新冠状病毒新在哪里?如何检测它?
导读新冠状病毒2019-nCoV为单链正链RNA病毒,如何检测,来看这篇文章。
一、新冠状病毒(2019-nCoV)简介
在武汉发现的新冠状病毒2019-nCoV为单链正链RNA病毒。在分类学上,2019-nCoV属于网巢病毒目(Nidovirales)、冠状病毒科(Coronaviridae)、正冠状病毒亚科(Orthocoronaviridae)的Beta冠状病毒属(Betacoronavirus),同属中还包括SARSr CoV、MERSr CoV等其它可感染人类的冠状病毒。
通过报道的全基因组比对发现,2019-nCoV与SARSr CoV、MERSr CoV平均分别有~70%和~40%的序列相似性。且其与宿主细胞相互作用的spike基因(编码S-蛋白)有更大的差异性。
SARS病毒的 S-蛋白和MERS病毒S-蛋白分别通过与人ACE2蛋白或DPP4蛋白互作结合来感染呼吸道上皮细胞。在S-蛋白的宿主受体互作区(RBD区),2019-nCoV与SARSr CoV比较相近,但是与MERSr CoV差异较大,首先排除了2019-nCoV病毒S-蛋白与DPP4互作感染人的可能。
通过分子结构模拟计算发现,虽然2019-nCoV病毒S-蛋白中与人ACE2蛋白结合的5个关键氨基酸有4个发生了变化,但变化后的氨基酸,却整体性上非常完美的维持了SARS病毒S-蛋白与ACE2蛋白互作的原结构构象。
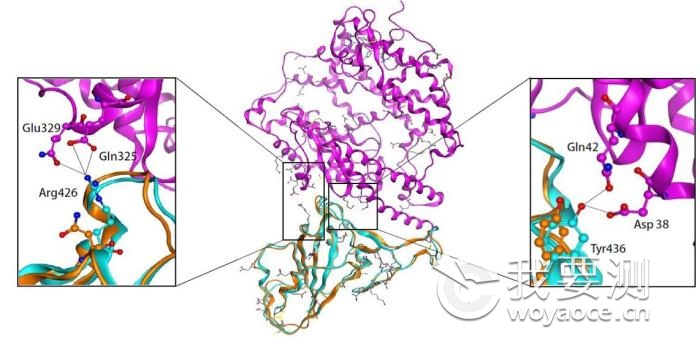
尽管武汉新型冠状病毒的新结构与ACE2蛋白互作能力,由于丢失的少数氢键有所下降(相比SARS病毒S-蛋白与ACE2的作用有下降),但仍然达到很强的结合自由能(-50.6 kcal/mol)。这一结果说明武汉冠状病毒是通过S-蛋白与人ACE2互作的分子机制,来感染人的呼吸道上皮细胞。
二、新冠状病毒(2019-nCoV)的检测
目前的检测都是基于提供的病毒基因组的测序,不同的公司和机构设计开发不同的检测试剂或测试盒,但基本原理和方法都大体一样。卫计委对这次新型新冠状病毒归为乙类传染病,但目前按甲类传染病控制。作为医学检测实验室要关注的是检测样品传送、检测和样本保存等的生物安全的控制,同时检测结果的确认和报告。
(一)送检样本的要求:
按照卫计委有关医学生物安全要求进行。根据生物安全相关规定,新冠状病毒2019-nCoV的送检样本需要满足以下要求:
1.样本:必须在符合生物安全规范的场所进行取样和包装;
2.容器:密封、无菌,耐高/低温度范围-40℃~55℃(如需液氮保存时需耐受 -196℃),耐压范围≥ 95 KPa,防水、防破损、防泄漏,生物危险性标识、提示说明、放置方向等信息完整清晰;
3.标签(贴在主容器外):类别、编号、名称、容量;
4.相关资料(置于防水袋内,贴于辅助容器外):数量、危险性申明、鉴定书、发送接收者信息。
(二) 检测指导原则:
1.应该在生物安全二级(BSL-2)以上级别设施中进行相关操作;
2.同时收集上呼吸道(URT)和下呼吸道(LRT)的标本,通过 RT-PCR 进行 2019-nCoV 核酸检测;
3.仅在无法使用 RT-PCR 时才建议使用血清学进行诊断;
4.对于疑似患者,特别是患有肺炎或严重疾病的患者,单个 URT 样本阴性不能排除2019-nCoV感染的可能,应增加LRT样本,LRT(相对于 URT)样本更可能呈阳性;
5.对于已经确诊 2019-nCoV 感染的患者,应重复收集样本(至少每 2-4 天收集一次),以证实病毒清除。直到患者出现两个连续的至少间隔 24 小时的全阴性结果(URT 和 LRT 样本均为阴性),可诊断临床康复。
(三)样本检测实验步骤:
对于新病毒的RT-PCR测试,不同来源的试剂盒要求的实验操作不尽相同,应根据试剂盒说明书要求进行操作。
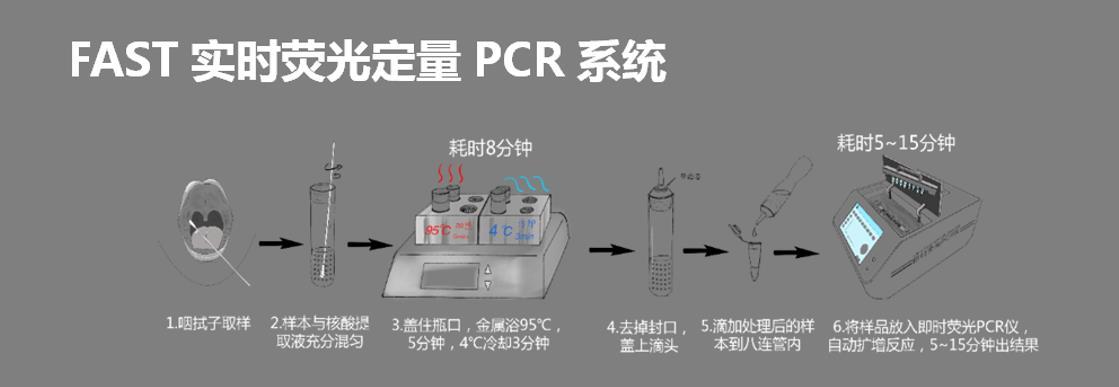
以下是典型的RT-PCR操作步骤:
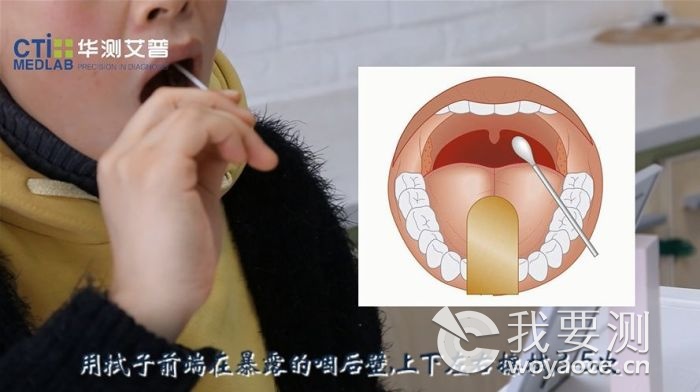
1.取样(URT 和 LRT 样本);
2.取适量样本与核酸提取液充分混匀;
3.对混合液进行金属浴,95℃温育5 min,4℃冷却3 min;
4.对处理后的混合液进行实时荧光检测。
三、检测相关的仪器及材料
(一)相关的仪器设施
1.实时荧光PCR仪
2.全自动核酸分离系统
3.高压灭菌锅
4.生物安全柜(符合要求的)
5.冷冻离心机(10000转/分以上,气溶胶防护操作)
6.移液枪 (气溶胶防护操作)
7.符合生物安全要求的隔离条件实验室或区域。
(二)检测试剂
1.病毒核酸检测荧光试剂(或试剂盒)
2.核酸提取试剂(或商业化的提取试剂盒)
3.RT-PCR试剂
(三)相关器材
1.TIP头,离心管,手套,联排PCR管等。
2.人的安全防护:防护服、手套、N95口罩、 防护眼罩。生物安全消毒袋、有效的消毒液。
以上简要介绍,供参考。
作者简介:朱金国,男,研究员,毕业于武汉大学病毒学及分子生物系,长期从事检测技术工作。















评论