FDA官宣SGS为510(K)外科口罩第三方审核机构!
SGS纺织及鞋类服务 2020-12-22 点击 285 次
导读美国食品和药物管理局(FDA)将暂时取消对某些口罩和呼吸器的要求,以增加其在市场上可获得的机会。
因在新型冠状病毒(COVID-19)流行期间,各类医用个人防护设备持续短缺,美国食品和药物管理局(FDA)将暂时取消对某些口罩和呼吸器的要求,以增加其在市场上可获得的机会。
510(k)要求
对于医疗用口罩,只要确保口罩产品不给用户带来不必要的风险,FDA暂时取消完整的监管要求,包括向FDA提交510(k)上市前许可的申请,增加该类口罩在市场上可获得的机会。
FDA表示,如果属于II类医疗器械的外科口罩满足液体阻隔性能和阻燃性标准,并且带有准确的标签,则允许该类口罩在没有510(k)的许可下仍可流通使用。
按正常程序,制造商必须获得510(k)的许可才能上市一次性医疗器械。但鉴于对外科口罩和呼吸器的迫切需求,FDA宣布将与不同公司合作以加快紧急使用授权(EUA)流程,并为这些申请者提供符合EUA申请要求的详细信息清单。
SGS获FDA认可
本月初,SGS被FDA认可为510(K)外科口罩第三方审核机构(官方公告如下)。
官网信息
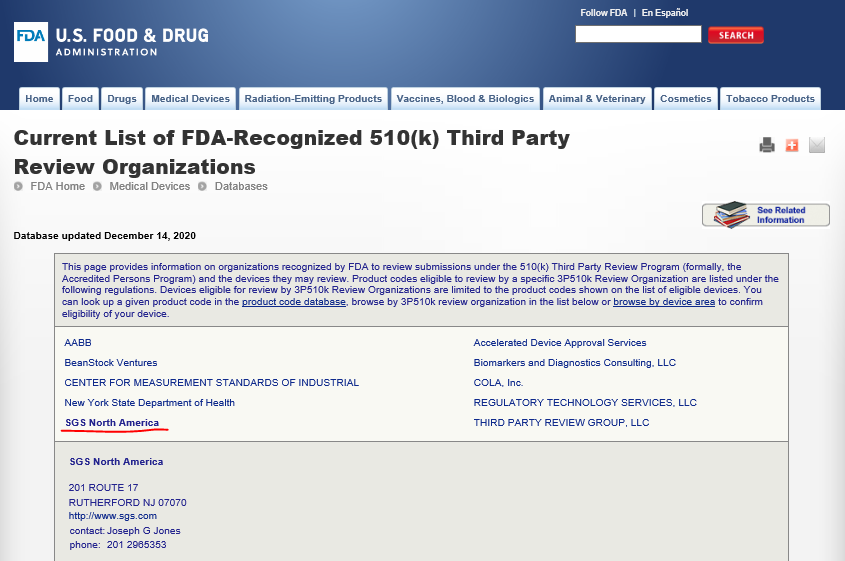
欲了解更多,点击进入 SGS通标标准技术服务有限公司 >>
编辑:张圣斌
[来源: SGS纺织及鞋类服务]
相关资讯
会员动态
-
 关于召开2024’第八届材料与试验高端论坛的通知(第一轮)钢研纳克检测技术股份有限公司 2024-09-30
关于召开2024’第八届材料与试验高端论坛的通知(第一轮)钢研纳克检测技术股份有限公司 2024-09-30 -
 第五届中国新材料产业发展大会 —— CY-09 材料产业高质量发展论坛 诚邀您投稿并参会钢研纳克检测技术股份有限公司 2024-09-29
第五届中国新材料产业发展大会 —— CY-09 材料产业高质量发展论坛 诚邀您投稿并参会钢研纳克检测技术股份有限公司 2024-09-29 -
 喜讯丨中纺标携手得物App共筑品质新高度,服装鞋靴品质保障中心揭牌成立中纺标检验认证股份有限公司2024-09-27
喜讯丨中纺标携手得物App共筑品质新高度,服装鞋靴品质保障中心揭牌成立中纺标检验认证股份有限公司2024-09-27 -
 关于举办 2024 测量科学与产业计量测试技术报告会 — 新材料计量测试技术分会的通知钢研纳克检测技术股份有限公司 2024-09-27
关于举办 2024 测量科学与产业计量测试技术报告会 — 新材料计量测试技术分会的通知钢研纳克检测技术股份有限公司 2024-09-27 -
 CTI华测检测上海化妆品功效评估中心正式投入运营,聚力前行推动产业谋变破局华测检测认证集团股份有限公司2024-09-27
CTI华测检测上海化妆品功效评估中心正式投入运营,聚力前行推动产业谋变破局华测检测认证集团股份有限公司2024-09-27
最新送检订单
药用复合膜异常毒性检测
塑性指数、耐火度检测
检测防割手套 ANSI
化验养发乳是否含有硝酸银?
最新特色检测
近期会议











评论