
领域分类:医药-药物研发和生产服务-其他
检测项目:药物研发
自2018年,部分沙坦类药物中二甲基亚硝胺杂质超标召回事件后,亚硝胺杂质污染药品安全问题越来越引起了全球药品监管的关注,而近2年全球药品监管机构监管重点转向了由药物本身相关的亚硝胺杂质上。
截至2022年底被召回的药品种类超过20种,其中包括: 缬沙坦、氯沙坦、厄贝沙坦、雷尼替丁、尼扎替丁、二甲双胍、利福平、伐尼兰克、普萘洛尔、喹那普利苯海拉明……
明捷医药痕量分析团队积累了丰富的亚硝胺研究经验,已经完成超过50种产品亚硝胺杂质研究,本文将从12种亚硝胺杂质快速筛查、西格列汀中NTTP检测、普萘洛尔中N-亚硝基普萘洛尔检测等项目案例抛砖引玉,共探药物中亚硝胺杂质的研究。
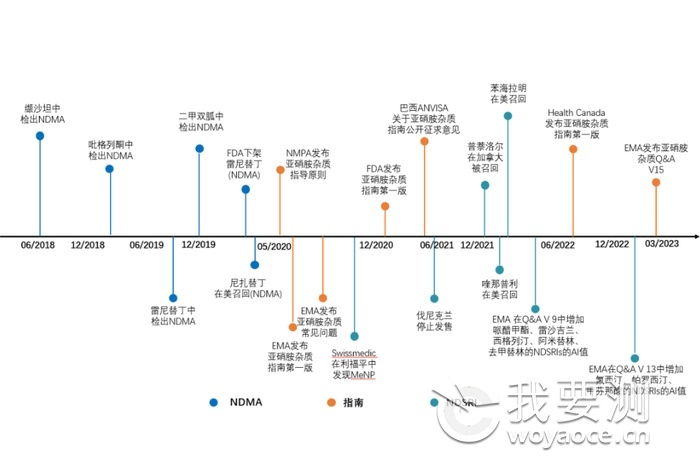
根据ICH M7 基因毒指导原则中,亚硝胺被归为“关注列队”,已有研究数据表明带有亚硝胺结构的化合物,大部分具备致癌性。因此中美欧多国药品监管机构在2020年陆续出发亚硝胺杂质研究相关指南,从而更多的亚硝胺杂质在药品中被不断发现。
近2年全球药品监管机构监管重点转向了由药物本身相关的亚硝胺杂质上,这些亚硝胺杂质的形成和药物活性成分密切相关,即被称为亚硝胺药物成分相关杂质(Nitrosamine Drug Substance-Related Impurites, NDSRI)。 NDSRI就是那些由药物本身自带的仲胺(或叔胺)结构单元及相关杂质与辅料中的亚硝酸盐转化产生的亚硝胺,同时NDSRI可能是制剂处方相关的降解杂质,需要考察产品效期NDSRI含量。 NDSRI亚硝胺杂质通常没有明确确定的允许摄入量(Allowed Intake, AI),为此FDA和EMA给NDSRI设定了苛刻的AI值。如FDA 指定的临时 AI为 26.5 ng/天;EMA为新的 NDSRI 设定了 18 ng/天的临时 AI。随后EMA引入了 178 ng/天的临时 AI,直到数据可以证明其确切的AI。这种临时AI的使用时间为1年过渡期。 亚硝胺杂质已成为全球制药行业头上的达摩克利斯之剑,威胁着上市药品的质量与患者的用药安全。 接下来我们将从以下三个项目案例,与大家共探药物中亚硝胺杂质的研究。
12种亚硝胺杂质快速筛查
目前已有7个小分子亚硝胺被FDA列入“关注列表”,其来源多样,包括原料药,辅料,甚至制药用水。所以,对制药用水中小分子亚硝胺杂质的筛查,对于亚硝胺杂质的来源调查和机理探究就显得尤为重要。明捷医药基于LCMSMS系统,建立了注射用水、纯化水、饮用水中12种小分子亚硝胺杂质快速检测方法,包括了“关注列表”中的7个亚硝胺,其LOQ均≤10 ppb。

西格列汀中NTTP检测
2022年8月,FDA公告由于在部分西格列汀制剂中发现NTTP杂质,要求相关企业对产品进行检测。FDA公布的NTTP的AI≤37ng/day,同时为了防止药物短缺,临时性的将AI放宽至246.7ng/day,并要求检出量超过0.37 ppm时应报告FDA。明捷医药在LCMSMS系统上,建立了西格列汀原料药和制剂中的NTTP检测方法,能有效定量0.037 ppm的NTTP含量。

普萘洛尔中N-亚硝基普萘洛尔检测
2022年3月,加拿大政府公告要求相关企业对部分普萘洛尔缓释制剂进行召回,原因是检出超过可接受限度的N-亚硝基普萘洛尔杂质。明捷医药使用LCMSMS系统建立了LOQ≥0.015ng/ml的N-亚硝基普萘洛尔杂质检测方法,同时研究了不同的样品制备过程对制剂检测结果的影响,排除检测过程中人为(原位)形成的亚硝胺杂质对结果的干扰。

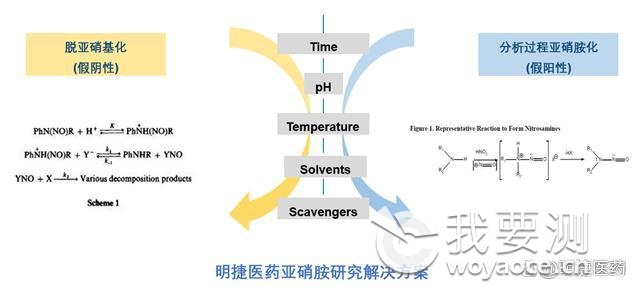
明捷医药痕量分析团队积累了丰富的亚硝胺研究经验,已经完成超过50种产品亚硝胺杂质研究,帮助客户完成中国、美国、英国、欧盟、WHO、韩国、日本等众多药品监管机构要求提交的产品亚硝胺风险评估及亚硝胺杂质方法开发验证及检测等研究工作,特别是亚硝胺产品检测过程中的“假阴性”与“假阳性”的研究。
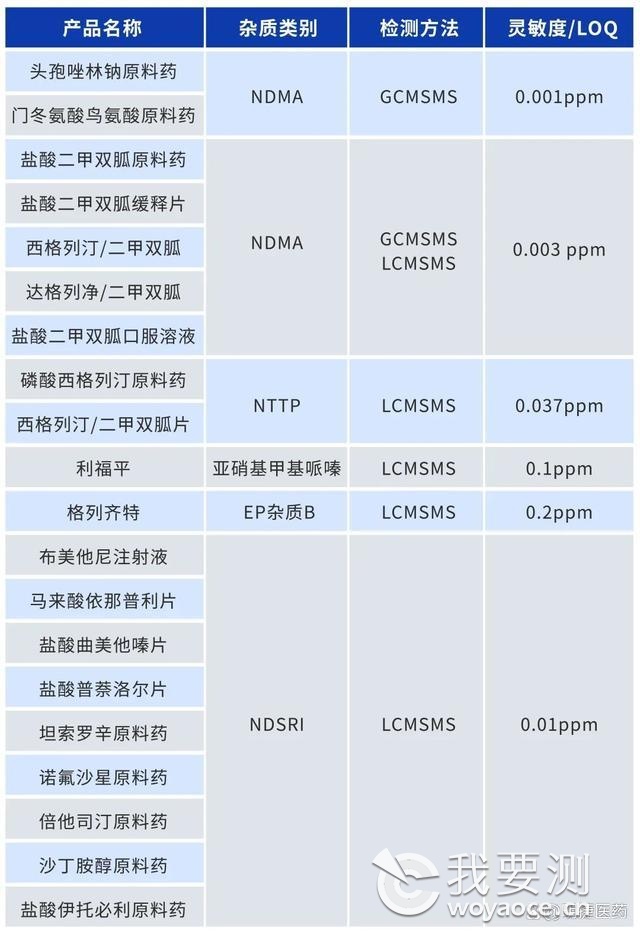
▲表 1:明捷已经建立平台检测方法部分清单
明捷服务
亚硝胺杂质风险评估报告
基于明捷现有平台方法的样品检测
项目专属亚硝胺杂质方法开发及检测
满足不同监管要求的方法验证及方法转移
前体杂质筛查:亚硝酸根与小分子仲胺杂质
亚硝胺杂质来源调查与亚硝胺杂质形成机理研究
| 产品名称 | 检测标准 | 检测项目 |
| 医药检测 | 定制服务 | 亚硝胺杂质 |
关于我们
明捷医药(药明康德控股子公司)以助力全球客户全面提升医药健康产品质量标准为愿景,持续致力于建立和完善符合全球医药健康产品政策法规的质量研究技术平台为使命,力求成为能力最全,技术最强,质量最好的行业领导者,为客户提供最优质的服务。
业务能力覆盖:小分子创新药及仿制药产品、多肽及蛋白产品、细胞与基因治疗产品、医疗器械与药械结合产品、原辅包及生产系统支持、质量体系与精益运营咨询等,为客户提供一体化的产品上市研究策略,支持客户产品全生命周期的研发、申报、上市后变更及质量维护,加速全球市场开拓。
下一篇:辅料中亚硝化试剂测定
上一篇:创新药CMC研究一体化服务






