
领域分类:医药-药物研发和生产服务-其他
检测项目:药物研发
创新药是时代发展的产物,随着医学发展、疾病克服而不断迭代。
2017年起,中国创新药产业政策支持力度加大,中国药品监管部门发布多项政策,创新药产业发展的政策环境随之显著改善。药物创新的鼓励、审评审批的加快、上市许可人制度的推行、临床实验数据核查、医保结构性控费等,都为我国创新药的研发和生产打了一剂强心针,未来几年将是各药企创新药密集获批上市的黄金期。而如何提高药物研发效率和降低研发成本,已经成为药物研发领域的主要挑战。
明捷医药成立至今,在创新药CMC研究的赛道上不断提升专业化优势并完善质量合规体系,从而提高交付物的质量及加快交付周期,为创新药公司极大程度节省成本并缩短IND/NDA申报周期。
屹今为止,明捷已经承接并完成近40+个NCE分子的质量研究服务。建立了完善的符合国际国内申报要求的创新药IND/NDA服务策略及流程。
适用范围(创新药CMC研究服务)
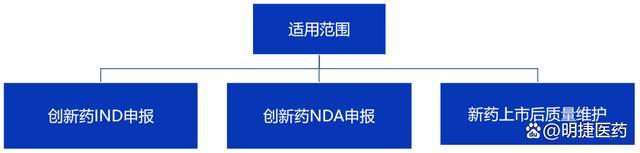
服务内容
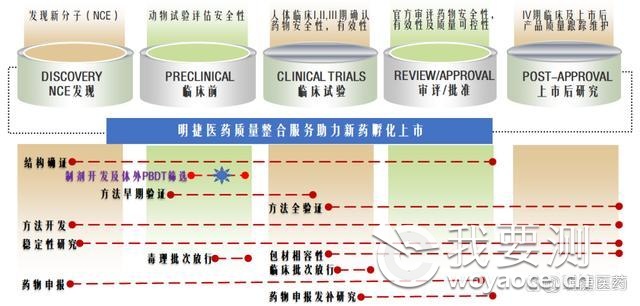
参照ICH Q1~Q14质量研究指南,并结合国家食品药品监督管理总局发布的《化学药品注册分类及申报资料要求》,对于创新药IND/NDA申报,明捷制定了一系列创新药CMC研究策略和流程,服务内容汇总如下:

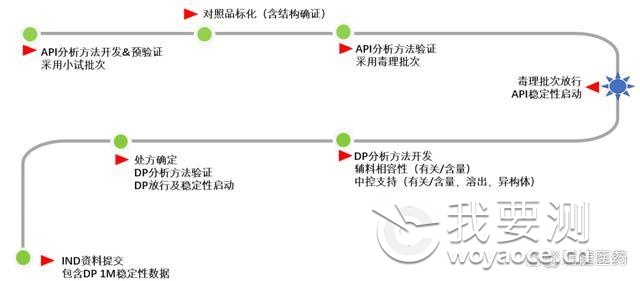
流程示例(创新药IND申报,~10个月)
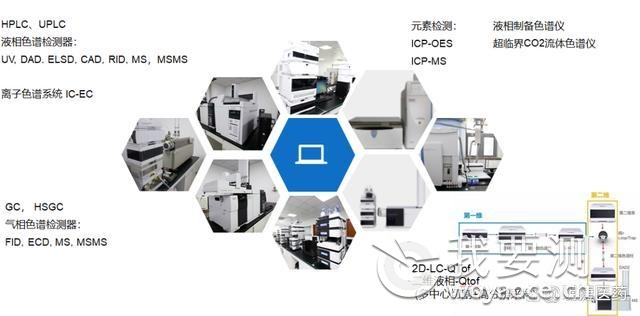
多样化的杂质研究手段
专业的降解杂质预测软件

符合M7规则的化合物遗传毒性预测软件

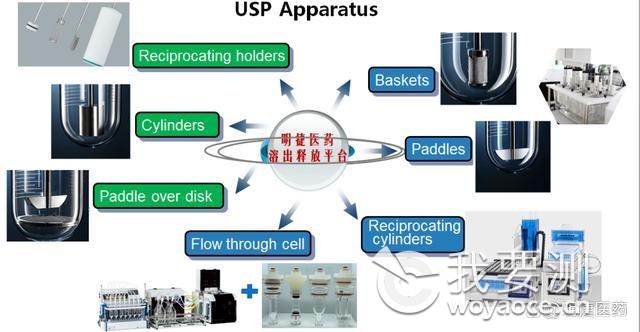
全面的溶出释放平台
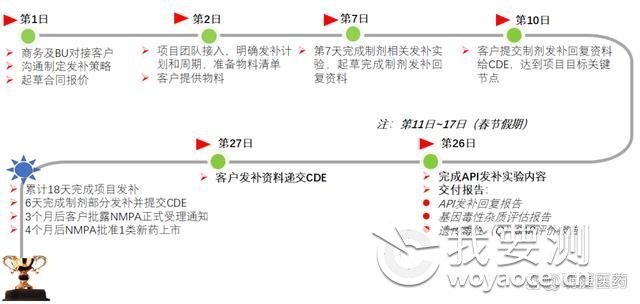
NDA阶段原料药+制剂杂质发补案例(18天完成)
| 产品名称 | 检测标准 | 检测项目 |
| 创新药 | 定制服务 | CMC |
明捷医药(药明康德控股子公司)以助力全球客户全面提升医药健康产品质量标准为愿景,持续致力于建立和完善符合全球医药健康产品政策法规的质量研究技术平台为使命,力求成为能力最全,技术最强,质量最好的行业领导者,为客户提供最优质的服务。
业务能力覆盖:小分子创新药及仿制药产品、多肽及蛋白产品、细胞与基因治疗产品、医疗器械与药械结合产品、原辅包及生产系统支持、质量体系与精益运营咨询等,为客户提供一体化的产品上市研究策略,支持客户产品全生命周期的研发、申报、上市后变更及质量维护,加速全球市场开拓。
下一篇:全球申报亚硝胺杂质研究
上一篇:药物晶型定性与定量方法学研究






