
药物杂质分析检测
资质:
适用范围:
领域分类:医药-药物临床前研发和安全性评价-其他
检测项目:药物杂质
详情介绍:
服务背景
我的优势
药物杂质的来源分析
药物中的杂质可能来源于药物生产以及销售等各个环节。根据 ICH指导原则可将药物杂质分为有机杂质、无机杂质、残留溶剂以及其他杂质。
对药物杂质研究时引入“质量源于设计( Quality byDesign,QbD)”的理念,可在药物生产之前根据具体工艺的合成机制、起始物料及各中间体的基本结构,初步勾画出产品的杂质谱。
杂质来源分析是制定药物杂质控制策略的基础,尤其是在对毒性杂质来源分析时,应分析所有合成和生产工艺中的试剂、中间体、副产物,推测可能产生的潜在杂质以及分析实际存在的杂质。在原料药合成结束后,药物的活性化合物虽然经过毒性分析已不含有“警示结构”(alerting structure),但是在生产过程中使用到含有警示结构的化合物则还需考虑其遗传毒性。
药物杂质分析技术
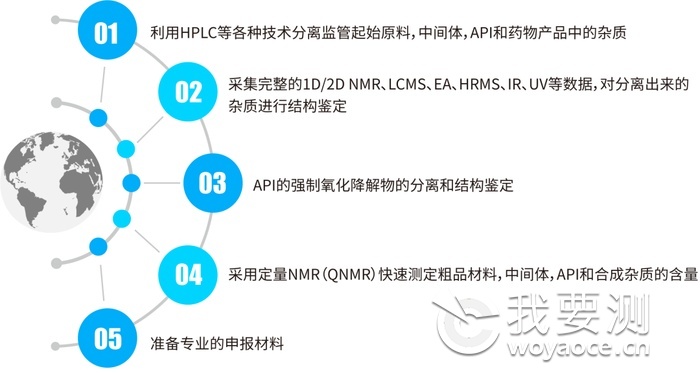
药物杂质分析方法

| 产品名称 | 检测标准 | 检测项目 |
| 药物杂质 | GB/T 34800-2017 | 蛋白酶K酶活力及杂质检测方法 |
| 药物杂质 | GB/T 23182-2008 | 饲料中兽药及其他化学物检测试验规程 |
| 药物杂质 | GB/T 9722-2006 | 化学试剂 气相色谱法通则 |
| 药物杂质 | SN/T 4810-2017 | 进出口食用动物β-内酰胺类药物残留量的测定 放射受体分析法 |










